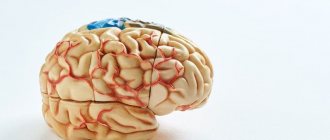
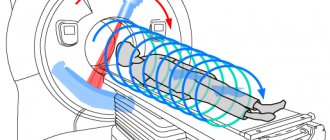
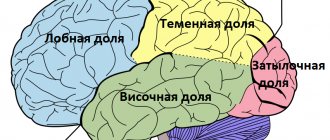
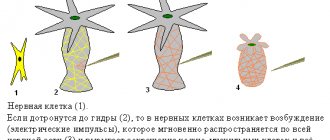
Кортикальная атрофия головного мозга – это разрушительные необратимые изменения, которым чаще всего подвержены люди от 50 до 55 лет, хотя есть случаи кортикальной атрофии и у новорожденных младенцев. Патологические нарушения, как правило, проявляются в лобных долях головного мозга, которые отвечают за процесс мышления, поведение человека, контроль. Болезнь протекает медленно с постепенным нарастанием основных симптомов, что в конце концов приводит к возникновению и развитию старческого слабоумия.
Причины лейкомаляции
Головной мозг недоношенных новорожденных очень чувствителен к недостатку кислорода, так как компенсаторные механизмы еще не развиты, и микроциркуляторное русло не может своевременно обеспечить доставку крови. У доношенных детей с более или менее зрелой нервной системой и кровотоком гипоксия стимулирует кровообращение, поэтому повреждения не будут так выражены.
Вариант развития внутриутробной гипоксии (кислородного голодания) из-за недостаточности плацентарного кровотока
Проблема усугубляется еще и тем, что у недоношенных детей нет хорошей связующей сети между артериями мозга, и особенно страдает при этом подкорковый отдел вокруг желудочков, на расстоянии до 1 см от их стенок, больше в теменных зонах. Этим объясняется именно перивентрикулярное (около желудочков) расположение очагов некроза.
Гипоксия вызывает образование свободных радикалов, кислых продуктов обмена, которые не только оказывают непосредственное повреждающее действие на нейроны, но и способствуют нарушению микроциркуляции в виде тромбозов, застоя крови в мелких артериях и венах. Таким образом, гипоксия, сама по себе вызывающая некроз, провоцирует метаболические расстройства и тромбозы, которые еще больше усугубляют ситуацию.
Замечено, что перивентрикулярная энцефалопатия чаще развивается у малышей, находившихся на искусственной вентиляции легких (ИВЛ). Казалось бы, аппарат обеспечивает дыхание и доставку кислорода, поэтому головной мозг страдать не должен. Однако, избыток кислорода, подаваемый через аппарат, провоцирует спазм артериол, который приводит к ишемии.
Частота ПЛ среди новорожденных зависит от времени года. Обычно большее число таких пациентов приходится на зимне-весенний период. Возможной причиной считают недостаток витаминов и влияние неблагоприятных метеоусловий на организм беременной в поздние сроки гестации.
Факторами риска лейкомаляции считают:
- Тяжелые гестозы;
- Хронические инфекции у беременных;
- Внутриутробная гипоксия из-за нарушений в плаценте или кровотоке у плода;
- Аномалии родов – преждевременные роды, преждевременное излитие вод, слабость родовых сил;
- Патология новорожденных – респираторный дистресс-синдром, пневмонии, требующие проведения ИВЛ.
Поражение головного мозга. Перивентрикулярный геморрагический инфаркт (ПГИ)
Поражение головного мозга. Перивентрикулярный геморрагический инфаркт
Перивентрикулярный геморрагический инфаркт (ПГИ), называемый также «распространенным красным размягчением», «венозным инфарктом», «церебральной геморрагической энцефалопатией», «перивентрикулярным геморрагическим поражением» и «геморрагической перивентрикулярной лейкомаляцией», встречается преимущественно у глубоко недоношенных детей (20—35 недель беременности) и возникает в результате нарушения оттока крови (стаза-тромбоза) в системе внутренних мозговых вен. При тромбозе вены Галена возникают массивные билатеральные геморрагические размягчения полуовальных центров. Однако чаще встречаются менее значительные поражения. ПГИ часто наблюдаются у детей с инфекциями, которые играют важную роль в их патогенезе.
Термин ПГИ еще не вошел в широкую практику клиницистов, которые чаще используют понятие «перивентрикулярное кровоизлияние» (ПВК). Так, при НСГ-исследовании у детей с перинатальными поражениями ЦНС ПВК обнаруживаются в 11 % случаев. Вероятно, часть ПВК — это ПГИ, другая же часть может быть представлена перивентрикулярными ВМК и ОГЛ.
Макроскопическое исследование: в перивентрикулярных областях боковых желудочков обычно в симметричных отделах обнаруживаются обширные участки дряблой ткани темно-красного цвета. ПГИ — это не простое кровоизлияние, это «пропитывание» кровью перивентрикулярного белого вещества мозга в сочетании с его отеком и неполным некрозом.
По периферии поражений выявляются гипертрофированные астроциты, тучные астроциты Ниссля и иногда очаги ПЛ. В ранней фазе процесса вокруг кровоизлияний обнаруживаются гибнущие глиоциты (скорее всего, олигодендроциты), ядра которых приобретают формы крючков и запятых.
В субэпендимальных и корковых венах, а также в областях инфарктов нередко обнаруживаются тромбы. Вокруг кровоизлияний могут выявляться единичные лейкоциты. ПГИ, в отличие от ВМК, является билатеральным, симметричным и в большей или меньшей степени вовлекает все доли мозга. Изредка процесс распространяется на весь полуовальный центр.
ПГИ может быть причиной смерти. ПГИ обычно сочетаются с СЭК, ишемическими поражениями нейронов коры и ствола мозга.
Микроскопически определяются многочисленные кроной.шил ния, нередко вокруг тромбов мелких сосудов, чередующиеся с участками отека и фокусами некробиоза мозговой ткани ПГИ может осложниться внутримозговым кровоизлиянием (гематомой) и ВЖК. У выживших детей на месте ПГИ образуются многочисленные кисты с гемосидерозом и глиоз белого вещества мозга.
Вопросы этиологии, патогенеза и клиники ПГИ еще в начальной стадии изучения. Поэтому следует остановиться на исследовани ях А. Товбина, посвятившего ПГИ наибольшее количество работ. Автор выделяет «перивентрикулярные венозные инфаркты» у недоношенных детей и «корковые инфаркты» у доношенных новорожденных.
Он считает, что в результате анте- и интра- натальной гипоксии или дыхательных нарушений у новорожденных (гиалиновые мембраны, пневмония) возникают циркуляторные нарушения в головном мозге с венозным застоем и стазом-тромбозом в венах, которые ведут к геморрагическим некрозам мозга и внутри- желудочковым кровоизлияниям. Перивентрикулярную лейкомаляцию А.
Товбин рассматривает как одну из форм инфарктов или как микроинфаркты. Автор полагает, что, когда гипоксия и нарушения мозгового кровообращения менее выражены, в перивентрикулярных участках мозга возникают небольшие повреждения в виде двух форм: фокусов кровоизлияний в субэпендимальном матриксе и фокусов перивентрнкулярной лейкомаляции.
Патогенез их такой же, как и больших геморрагических венозных инфарктов. Поскольку очаги ПЛ нередко обнаруживались вокруг геморрагических инфарктов, то А. Товбин называет их «спутниками» последних. Таким образом, хотя А. Товбин рассматривает ПЛ в рамках венозных инфарктов, но он все же дифференцирует эти два вида некрозов.
Венозные геморрагические инфаркты резко отличаются от ПЛ уже макроскопически: представляют большие поля дряблой мозговой ткани, пропитанной кровью. В то же время их следует дифференцировать с таким осложнением, как массивные кровоизлияния в очаги ПЛ.
У выживших детей в областях ПГИ формируются глиоз и кисты, расширяются боковые желудочки мозга. Развивается ДЦП с гемиплегией, квадриплегией и задержкой психического развития.
Проблемы терминологии. Следует отметить, что, описывая рас-сматриваемое поражение, другие авторы используют иные термины. Так, С. В. Courville называет подобный патологический процесс «распространенным красным размягчением» и «церебральной геморра-гической энцефалопатией», считая его смертельным поражением, быстро приводящим к смерти. R. L.
Friede отмечает, что при тромбозе вены Галена возникают массивные билатеральные геморрагические размягчения в полуовальном центре. J. К. Larroche описывает перивентрикулярные геморрагические инфаркты в разделе мозговых кровоизлияний, связывая их с лейкомаляцией или с ишемией глубоких отделов белого вещества полушарий мозга. J. В. Wigglesworth, К. Е.
Раре считают, что перивентрикулярные венозные инфаркты в большинстве случаев являются вторичными по отношению к массивным субэпендим алы шм кровоизлияниям. J. Volpe подобные поражения относит к «перивентрикулярно-внутрижелудочковому кровоизлиянию».
Поражения, имеющие вид перивентрикулярных геморрагических инфарктов, называют также «геморрагической перивентри- кулярной лейкомаляцией», к которой относят случаи сочетания ПЛ с кровоизлияниями различных размеров. Таким образом, налицо не только терминологическая путаница, но и недостаточное понимание сущности рассматриваемого патологического процесса.
Полагаю, что ПГИ следует дифференцировать с перивентрикулярными ВМК, а также со случаями кровоизлияний в очаги перивентрикулярной лейкомаляции.
Источник: https://oborudka.ru/handbook/87.html
Что происходит в мозге при лейкомаляции?
При лейкомаляции головного мозга в подкорковых структурах появляются очаги некроза, обычно – коагуляционного, гибнут нервные клетки, а дефекты замещаются размножающимися клетками микроглии наподобие того, как образуются рубцы в других органах. Нейроны не могут размножаться, и поля омертвения мозгу нечем заполнить, поэтому следствием их становятся кисты (полости) – кистозная лейкомаляция.
Более половины случаев ПЛ сопровождаются вторичными кровоизлияниями в зоне ишемии и некрозов, возможны кровоизлияния в желудочки мозга. Важно, что кора мозга у таких детей поражается крайне редко в связи с хорошим кровоснабжением.
Лейкомаляция начинается в первые дни и продолжается около недели с момента рождения. Возможно и более позднее ее возникновение, обычно связанное с инфекцией или нарушением дыхания у новорожденного ребенка. В этих случаях на фоне уже имеющихся некрозов могут появляться новые, а состояние ребенка будет прогрессивно ухудшаться.
Очаги мультифокальной лейкомаляции диаметром в 2-3 мм обнаруживают в теменных и лобных долях, симметрично, вокруг стенок боковых желудочков. Реже поражаются височные и затылочные доли мозга. Исходом некроза становится образование множества кист разных размеров, рассеянных по подкорковому слою мозга (кистозная дегенерация), число которых со временем увеличивается. При тяжелой ПЛ они занимают всю перивентрикулярную часть полушарий.
Пытаемся разобраться в результатах МРТ ГМ
Пытаемся разобраться в результатах МРТ ГМ
- Doc
- 11-09-2015
- Справочник ВСДшника
О сколько нам открытий чудных готовит… МРТ. Заключение: очаги в белом веществе.
Что это за фигня такая и чем она грозит
Итак, для начала напомню, что сделать МРТ головного мозга меня побудили нехорошие симптомы, которые не прекращались на протяжении трех месяцев.
Попробую описать симптомы:
Системное, почти не прекращающееся легкое головокружение, почти незаметное, но очень неприятное.Постоянная “затуманенность” восприятия окружающего, “прибитость” и заторможенность в голове – лучше описать не могу.Иногда “заносило” на поворотах, мог “не вписаться” в дверной косяк, задеть угол стола и т.д.
Не часто, но, как говорится, обратил внимание.Довольно заметно ухудшилась трудоспособность – напомню, что мой основной инструмент – компьютер. Работать стало тяжело, не то слово…Хроническая усталость – к концу дня вообще ничего делать не получается, только гонять нехорошие мысли о своем никчемном здоровье.
Проблемы со сном – начал периодически рано просыпаться и больше заснуть не удавалось. В моем случае рано – это 5 утра, обычно спал до 6.30 – 7 утра. Ложусь довольно рано, в 23:00 и кто-то скажет что этого вполне достаточно, но я-то знаю сколько мне надо… Стал очень чувствителен к “недосыпу”.
Кстати, хроническое раннее пробуждение – это одна из основных жалоб и по сегодняшний день, только стало еще хуже. Но об этом будет отдельная история…Периодические, но не частые и не сильные головные боли.
Довольно продолжительные (2-5 часов), преимущественно в области полушарий и лобной части, затылочных болей не было.
Вот с таким “набором” я решил отправиться на МРТ головного мозга. Почему сразу на МРТ без всяких направлений от невролога? Скорее всего сыграл роль тот факт, что как раз незадолго до того, как у меня появились эти симптомы моя бывшая жена умерла от рака. Немного другая история и довольно длинная, всю её я рассказывать не буду, скажу только что касается темы МРТ.
Так вот, насколько я в курсе, её жалобы очень напоминали мои: никаких “диких” головных болей, головокружение, шаткая походка и т.д. В итоге по результатам МРТ ГМ у нее диагностировали опухоль (или метастаз в ГМ, точно не скажу). Вот я и решил, что прежде, чем появиться у невролога надо бы “расставить точки над И”, что я и сделал.
Страшно было – словами не передать!
Теперь результаты. Заключение МРТ (2007 год) гласит: МР-картина единичного очага в белом веществе головного мозга – вероятно сосудистого генеза. Признаки умеренно выраженной наружной гидроцефалии. Для общей картины приведу скан полного текста результата исследования:
Врач, который писал заключение ничего “военного” в исследовании не нашел, никаких опухолей и новообразований не увидел. По поводу “Единичного очага в белом веществе” круглых глаз не сделал, сказал, что скорее всего результат гипертонического криза или вообще врожденное, грозить особо ничем не может и причиной моих головокружений служить вряд ли может.
Уже потом, рассматривая дома результаты МРТ, сохраненные на DVD я нашел в своей голове вот такую “черную дыру”:
На приеме у невролога картину прояснить, в общем-то, не удалось. Никаких конкретных комментариев ни по поводу единичного очага, ни по поводу гидроцефалии, ни даже по поводу “черной дыры” я не получил. Все в общих чертах, типа “ничего смертельного”. Общие рекомендации и т.д. и т.п.
Причем побывал у двух неврологов. Прописали церебролизин, витамины и успокоительные. Сказали периодически наблюдаться и делать МРТ примерно раз в два года для наблюдения в динамике. Вроде бы и успокоили, но с другой стороны никаких конкретных мер.
Докторам, конечно, виднее, но настораживает.
Никаких изменений, а тем более улучшений моего состояния не последовало. Проходил назначенные курсы – впустую. На протяжении этих лет сделал еще 4 исследования МРТ ГМ. Картина почти не менялась. Приведу вырезки заключения МРТ (2012 год):
Несколько напрягала формулировка “единичные”, т.е. во множественном числе. Очередной визит к неврологу немного успокоил – практически никакой реакции на формулировку заключения я не увидел.
Вот последнее исследование, привожу его результаты полностью, т.к. заметил (на мой взгляд) очень нехорошую динамику. МРТ ГМ 2013 год:
Желтым маркером выделил пункт, который заставил меня поволноваться. На первых МРТ единичные очаги были 0.3см, а здесь уже фигурировала цифра 0.4 см.
Я, конечно, понимаю, что старею, со здоровьем лучше не становится, но все равно картина удручала. Очередной прием у невролога – опять ничего.
Увеличение очагов доктор объяснила “скорее всего погрешность или разная разрешающая спосбность аппаратов”. Ну вот что делать, приходится верить… Тем более, что это выгоднее, чем думать о плохом.
Плюс ко всему появилась липома межполушарной щели. Просто пипец какой-то…
Последний визит к неврологу закончился очередным курсом церебролизина (теперь внутривенно) и мексидола внутримышечно. Плюс 20 дней приема препарата Тагиста. Плюс к этому речь опять таки зашла об антидепрессантах. Но об этом потом…
В последний свой визит я задал доктору вопрос о рассеяном склерозе. Невролог категорически отрицал диагноз РС, но я все-таки расскажу почему я в очередной раз сделал МРТ и почему опять попал на прием к неврологу.
Думаю, что многие ВСД-шники проходили через подобные мучения и сомнения, так что в следующем посте поговорим немного о симптомах рассеянного склероза.
Источник: //xn--80acgb4aire.xn--p1ai/lib/25-head-mrt.html
Проявления лейкомаляции
Признаки лейкомаляции разнообразны и часто неспецифичны, но тяжелое гипоксическое повреждение мозговой ткани не может протекать бессимптомно. Выделяют несколько степеней ПЛ:
- Легкая степень – признаки поражения нервной системы сохраняются до недели от момента рождения;
- Средняя тяжесть – от 7 до 10 дней, возможны судороги, внутричерепная гипертензия, вегетативные нарушения;
- Тяжелая ПЛ – глубокое повреждение с угнетением головного мозга, нередко – кома.
Среди симптомов церебральной лейкомаляции возможны:
- Избыточная нервно-рефлекторная возбудимость или, наоборот, ее угнетение;
- Судорожный синдром;
- Гипотонус мышц;
- Стволовая симптоматика;
- Парезы и параличи;
- Зрительные нарушения в виде косоглазия;
- Задержка психомоторного развития, нарушения интеллекта, гиперактивность, дефицит внимания.
Специалисты особо отмечают, что неврологическая симптоматика в остром периоде и до 3-5 месяцев жизни может быть невыраженной. Примерно у 90% детей после острого периода наступает мнимое благополучие, длящееся до 5 и даже 8-9 месяцев жизни. И только по прошествии такого длительного времени возникают признаки дефицита нервной деятельности на фоне атрофии мозговой ткани.
Вокруг желудочков мозга сконцентрированы проводящие нервные пути, ответственные за двигательную функцию конечностей, поэтому основным признаком церебральной лейкомаляции у детей становится детский церебральный паралич, но степень выраженности его зависит от массивности некроза.
В связи с вовлечением ствола мозга, черепных нервов большая половина малышей страдает косоглазием, чаще – сходящимся, возможны нарушения глотания, дыхательные расстройства. К полугодовалому возрасту проявляется судорожный синдром. Чем больше размер полей некроза и, соответственно, кист, тем больше выражена мозговая недостаточность. Характер симптомов определяется локализацией очагов повреждения (двигательные, зрительные расстройства, судороги, задержка психического развития).
Тяжелое поражение теменных и лобных долей влечет детский церебральный паралич с одновременным нарушением психического развития. Если вовлечены лишь проводящие пути, отвечающие за иннервацию конечностей, то паралич может не сопровождаться нарушением интеллекта и развития ребенка.
Часто у детей, перенесших перинатальную гипоксию, среди симптомов фигурируют дефицит внимания и гиперактивность при сохранном моторном развитии. Это относительно благоприятный вариант патологии, который можно корректировать специальными лечебными мероприятиями.
Ввиду такой непредсказуемости и разнообразия симптомов, маме бывает сложно разобраться, чего ожидать, когда малыш родился раньше срока и в условиях гипоксии. Если поражение носит умеренный или тяжелый характер, то ребенок не будет развиваться соответственно возрасту – не научится вовремя переворачиваться, сидеть и, тем более, ходить. Речевое развитие затормозится, малыш не сможет гулять, не будет следить за игрушками и проявлять такого характерного для своего возраста любопытства.
Особое внимание привлекает гипертонус, который может быть болезненным, поэтому ребенок будет беспокойным, плаксивым, нарушится сон. Грудное вскармливание может стать проблемой из-за плохого сосательного рефлекса, избыточной нервно-мышечной возбудимости или атонии.
Недостаточная прибавка в весе, медленный рост, не соответствующий возрасту, и отсутствие навыков, которыми должен овладевать растущий ребенок – основные симптомы, с которыми приходится иметь дело родителям малыша с умеренной или легкой степенью повреждения подкорковых структур.
Примерно к году становится заметным неврологический дефицит, развивается церебральный паралич, задерживается психомоторное развитие. После года, когда восстановительный период подходит к концу, в клинике преобладают такие последствия, как задержка психоречевого развития, эмоциональная лабильность, проблемы со сном и вниманием, которые могут быть наряду с более тяжелыми моторными расстройствами (детский церебральный паралич).
ПЛ у взрослых может быть причиной церебрального паралича, гипертонуса, нарушений интеллекта, тяжелой олигофрении. При благоприятном течении патологии взрослые люди мало чем отличаются от остальных.
МРТ-диагностика многоочагового поражения головного мозга
[▼]:
рассеянный склероз
гипоксические энцефалопатии мигрень черепно-мозговая травма прогрессирующая мультифокальная лейкоэнцефалопатия острый рассеянный энцефаломиелит обратите внимание Актуальность
. В последние годы широкое внедрение новейших методов нейровизуализации расширило возможности изучения неврологических процессов, которыепроявляются многоочаговыми изменениями головного мозга. Дифференциальная диагностика таких изменений представляет значительные трудности. Высокая тканевая контрастность, возможность мульти-планарной визуализации, отсутствие лучевой нагрузки, неинвазивность делают магнитно-резонансную томографию (МРТ) методом выбора. Однако ряд сосудистых, воспалительных, инфекционных и наследственных заболеваний могут иметь схожую МРТ-картину.Термином «демиелинизирующие заболевания» (ДЗ) ЦНС принято называть первичные, как правило, идиопатические патологические процессы, вызывающие деструкцию нормально развитого миелина. Такие процессы, как сосудистая (дисциркуляторная, гипертоническая) энцефалопатия, васкулиты, ряд инфекционных заболеваний, нейротравма, дегенеративные заболевания нервной системы и многие другие, также вызывают потерю миелина проводящих путей, что сопровождается соответствующими изменениями сигнальных характеристик на МРТ. Но эти процессы имеют иную этиологию и патогенез, что не позволяет включить их в группу ДЗ.
► Рассеянный склероз
(РС) – хроническое, прогрессирующее заболевание ЦНС, проявляющееся рассеянной неврологической симптоматикой и имющее в типичных случаях на начальных этапах ремитирующее течение (Adams R., 1993).
МРТ обладает высокой чувствительностью в выявлении очагов РС, значительно превышая возможности как клинического обследования, так и других методов нейровизуализации.
Однако специфичность МРТ в диагностике РС составляет не более 80 %, что связано с тем, что очаги в белом веществе, сходные с очагами при РС, могут наблюдаться как у здоровых лиц, так и у пациентов, страдающих сосудистой энцефалопатией, мигренью, васкулитами, бактериальной и вирусной инфекцией и рядом других заболеваний.
В настоящее время международной группой экспертов в области РС приняты следующие ► критерии диагностики
рецидивирующее-ремиттирующего РС:
- 1
– один очаг, накапливающий контраст, или 9 очагов, гиперинтенсивных на Т2 ВИ;
2
– не менее одного инфратенториального очага;
3
– не менее одного субкортикального супратенториального очага;
4
– не менее трёх перивентрикулярных очагов.
Для диагностики требуется наличие не менее трёх перечисленных критериев. Эти критерии позволяют у ряда пациентов раньше диагностировать рассеянный склероз, чем стандартные способы диагностики клинически значимого рассеянного склероза. У многих больных уже на ранних стадиях заболевания при МРТ мозга выявляются множественные очаги, подтверждающие диссеминацию «в месте». Это могут быть очаги повышенной интенсивности на Т2‑взвешенных изображениях (особенно при использовании программы FLAIR) в белом веществе и черные «дыры» на Т1‑взвешенных изображениях, связанные с атрофией нервных волокон. При использовании контрастного усиления на Т1‑взвешенных изображениях можно выявить активные очаги, так как парамагнитный контраст накапливается в зонах повышения проницаемости ГЭБ и активного воспаления. Типичной локализацией очагов, чаще размерами 0,2 – 1,0 см, являются:
- ♦ мозолистое тело, ♦ перивентрикулярное белое вещество, ♦ могут быть инфратенториальные очаги (типично — вентральнее IV желудочка).
Иногда возможно распространение процесса и на серое вещество – на подкорковые ядра. Поражение чаще несимметричное, билатеральное. Бляшки РС, расположенные перивентрикулярно, имеют овальную форму и расположены перпендикулярно боковым желудочкам («пальцы Доусона»). Перифокальная реакция в виде отёка может быть слабой, только в «активной» фазе. Очаги при РС могут накапливать контрастное вещество, что отражает нарушения проницаемости гематоэнцефалического барьера. Возможно 3 типа контрастирования бляшек при РС (Пронин И. Н. и соавт.,2003):
- ♦ диффузный, ♦ кольцевидный ♦ частичный [].
► Гипоксические энцефалопатии
. У пациентов старше 40 лет мелкоочаговые поражения головного мозга возникают при гипоксических энцефалопатиях (дисциркуляторная энцефалопатия, болезнь Бинсвангера). Это связано с атрофией миелиновых оболочек, вызванной атеросклеротическим поражением артериол, и развивающейся вследствие этого хронической гипоксией. Этот процесс протекает асимметрично билатерально с локализацией как в глубоком, так и в субкортикальном белом веществе. Перифокальная реакция отсутствует. При контрастном усилении интенсивность МР-сигнала на Т1 ВИ не изменяется (нет накопления контрастного вещества).При дисциркуляторной энцефалопатии нередко развивается гидроцефалия, как внешняя (проявляется расширением субарахноидальных пространств), так и внутренняя (увеличение желудочковой системы), вследствие атрофии вещества головного мозга.
В отличие от демиелинизирующих процессов, при гипоксических энцефалопатиях имеются аналогичные изменения в базальных ядрах, зон глиозно-атрофических изменений после нарушений мозгового кровообращения по ишемическому типу или лакунарных инфарктов, визуализируются расширенные периваскулярные пространства Робена – Вирхова. Нередко перивентрикулярно определяется лейкоареоз (зоны диффузного повышения МР-сигнала на Т2 ВИ в режиме FLAIR вокруг боковых желудочков, чаще окаймляющие рога желудочков) [].
► Мигрень
. Мигрент характерна для пациентов молодого возраста.
При МРТ-исследовании определяются множественные, мелкие (до 0,5 см) округлые очаги, локализующиеся в белом веществе полушарий, иногда в подкорковых ядрах, не встречаются субтенториально.
Перифокальная реакция отсутствует, накопления контрастного вещества нет. Возникновение подобных глиозных изменений связывают с развитием васкулопатии мелких артериол [].
► Черепно-мозговая травма
. При черепно-мозговой травме могут наблюдаться множественные очаговые изменения вещества мозга. Чаще подобные очаги определяются при легкой травме по типу сотрясения мозга, но иногда и при тяжёлой нейротравме по типу ДАП (диффузное аксональное повреждение).
Очаги могут иметь различные размеры, локализуются чаще в валике мозолистого тела, мосту, среднем мозге. В острый период травмы для них характерно наличие геморрагического компонента.
В отдаленном периоде вокруг посттравматических очагов отсутствует отёк вещества головного мозга, нет накопления контрастного вещества [].
► Прогрессирующая мультифокальная лейкоэнцефалопатия
. Прогрессирующая мультифокальная лейкоэнцефалопатия развивается у лиц с врождённым или (чаще) приобретенным иммунодефицитом (СПИД, на фоне иммуносупрессивной терапии). Этиологическим фактором является реактивация латентной вирусной инфекции.
При МРТ-исследовании в белом веществе субкортикально визуализируются множественные очаги, от мелких до сливных, неправильной формы, с нечёткими границами на Т2 ВИ (слабый отёк). Типичная их локализация – теменно-затылочные доли, но могут быть в любых отделах мозга. Поражение двустороннее, асимметричное. Контрастное усиление очагов отсутствует, но, по данным ScottW.
, 2002, у 5 – 15 % больных возможно контрастирование по периферии [].
► Острый рассеянный энцефаломиелит
.
По данным МРТ, характерным признаком острого рассеянного энцефаломиелита (ОРЭМ) является наличие очагов демиелинизации, численность которых при последующих МРТ-исследованиях уменьшается за счет частичного или даже полного восстановления структуры ткани, в то время как при РС численность очагов и их размеры, а также активность накопления КВ изменяются на каждом этапе течения заболевания. Величины ИКД в нормальной ткани головного мозга пациентов с ОРЭМ незначительно отличаются от таковых у здоровых людей. На диффузионно-взвешенных изображениях очаги демиелинизации характеризуются повышением интенсивности МР-сигнала с возрастанием значений ИКД в белом веществе головного мозга [].
► Обратите внимание
. Наиболее информативным и перспективным методом диагностики многоочагового поражения головного мозга является МРТ.
Именно она дает возможность прижизненной визуализации многоочаговости поражения ЦНС при различных заболеваниях и в динамике позволяет судить о стадии процесса у конкретного больного.
Однако результаты МРТ, взятые изолированно (без учета клинической картины заболевания), не являются абсолютным критерием в постановке диагноза. Несмотря на то, что МРТ признана «золотым стандартом» нейровизуализации, протоколы МРТ-исследований постоянно совершенствуются и дополняются современными методиками [].
?
|
laesus_de_liro
Актуальность
. По данным А.А. Сотникова и О.Л. Минаевой (ГОУ ВПО Сибирский государственный медицинский университет Росздрава, г. Томск, 2008) около 70% женщин после выполнения онкологических оперативных вмешательств на молочной железе впоследствии нуждаются в проведении реконструктивно-пластических операций. Утраченную в ходе операции молочную железу восстанавливают с использованием свободного или несвободного TRAM-лоскутов или лоскута широчайшей мышцы спины с последующим эндопротезированием. Кроме реконструктивно-пластических операций, в настоящее время резко возросло количество пластических операций на молочной железе по поводу их эстетической коррекции. Среди этих операций в 39% случаев проводится редукционная маммопластика, в 44% случаев – аугментационная маммопластика и в 17% случаев выполняется коррекция формы соска или ареолы. Завершающим этапом реконструктивно-пластических и эстетических операций на молочной железе является сохранение или восстановление утраченного в ходе операции сосково-ареолярного комплекса (САК). Однако в 8-55% случаев реконструированный САК в отдаленном послеоперационном периоде становится малочувствительным и подвергается некротическим осложнениям. Поэтому так важно знать анатомо-топографическиме характеристики САК.
Иннервация
молочной железы (Кристиан Дж. Габка, Хайнц Бомерт, 2010) осуществляется
сегментарно
, латеральными ветвями 3 – 6 межреберных нервов (Т3 – Т6). Центральные отделы молочной железы, в том числе область соска и ареолы, получают сенсорную иннервацию из переднемедиальных и переднелатеральных волокон межреберных нервов Т3 – Т5; иннервация большей части молочной железы осуществляется за счет нерва Т4 (четвертого межреберного кожного нерва – г. anterior г. cutaneus lateralis IV п. intercostalis). При выполнении реконструктивно-пластических и эстетических операций на молочной железе настоятельно рекомендуется сохранить хотя бы один из указанных нервов для обеспечения сенсорной иннервации молочной железы. Нижние ветви шейного нервного сплетения также обеспечивают сенсорную иннервацию верхних отделов молочной железы. Медиальные, а также нижние отделы молочной железы иннервируются латеральными ветвями 2 – 6 межреберных нервов (Т2 – Т6). Латеральная кожная ветвь 2-го межреберного нерва (межреберно-плечевой нерв, n. intercostobrachialis) проходит латерально через подмышечную впадину и образует нервное сплетение с кожной ветвью срединного нерва (n. medianus), а также с 3-м межреберным нервом (Т3). Указанные нервы вместе обеспечивают иннервацию верхнемедиальных отделов плеча.
Практические рекомендации
. Сохранение данных нервов в ходе выделения подмышечных лимфатических узлов по поводу рака молочной железы в некоторых случаях может являться достаточно сложной задачей, поскольку нервы непосредственно проходят через центральную группу лимфатических узлов. Перед выполнением любого оперативного вмешательства на молочной железе целесообразно оценить чувствительность области соска с целью максимально раннего выявления нарушений иннервации в послеоперационном периоде. Интраоперационные травмы передне-медиальных и передне-латеральных сегментарных ветвей межреберных нервов могут обусловливать гипестезию вплоть до полной утраты чувствительности в после-операционном периоде. В ряде случаев иннервация может быть частично восстановлена с помощью массирования поврежденной области (противопоказано при онкологической патологии молочной железы).
© Laesus De Liro
Уважаемые авторы научных материалов, которые я использую в своих сообщениях!
Если Вы усматривайте в этом нарушение «Закона РФ об авторском праве» или желаете видеть изложение Вашего материала в ином виде (или в ином контексте), то в этом случае напишите мне (на почтовый адрес) и я немедленно устраню все нарушения и неточности.
Но поскольку мой блог не имеет никакой коммерческой цели (и основы) [лично для меня], а несет сугубо образовательную цель (и, как правило, всегда имеет активную ссылку на автора и его научный труд), поэтому я был бы благодарен Вам за шанс сделать некоторые исключения для моих сообщений (вопреки имеющимся правовым нормам). С уважением, Laesus De Liro.
Источник: https://laesus-de-liro.livejournal.com/205374.html
Лечение
Лейкомаляция сопровождается необратимыми изменениями нервной ткани, и какой-либо четкой схемы лечения этого состояния не разработано. Обычно врачи применяют симптоматический подход, в зависимости от конкретных проявлений патологии.
В качестве основного компонента лечения применяют ноотропные средства, помогающие улучшить кровоток и метаболизм в головном мозге (пирацетам, ницерголин, стугерон). Дополнительная терапия направлена на коррекцию двигательных расстройств, нарушений психомоторного развития.
В качестве профилактической меры акушеры-гинекологи предпринимают все возможные попытки пролонгирования беременности до того срока, когда роды станут безопасными для малыша. Если ребенок все же рождается недоношенным, то необходимо сразу же наладить контроль за дыханием и показателями гомеостаза – уровнем кислорода и углекислоты в крови, артериальным давлением, кислотно-щелочным равновесием.
Диагностика
Самым показательным методом исследования, который может выявить очаги демиелинизации головного мозга, является магнитно-резонансная томография. Характерная картина для данного заболевания – выявление очагов овальной либо круглой формы размерами от 3 мм до 3 см в каком-либо участке головного мозга. Типичной для локализации при данной патологии является область субкортикальных и перивентрикулярных зон. Если заболевание длится долгое время, то эти очаги могут сливаться. Также на МРТ видны изменения субарахноидальных пространств, увеличение желудочковой системы из-за атрофии мозга.
Относительно недавно для диагностики димеилинизирующих заболеваний стал применяться метод вызванных потенциалов. Оцениваются три показателя: соматосенсорные, зрительные и слуховые. Это дает возможность оценить нарушения в проведении импульсов в стволе мозга, зрительных органах и спинном мозге.
Электронейромиография показывает наличие аксональной дегенерации и позволяет определить деструкцию миелина. Также с помощью этого метода производят количественную оценку степени вегетативных нарушений.
Исследованиям иммунологического плана подвергается олигоклональные иммуноглобулины, содержащиеся в ликворе. Если их концентрация высока, это говорит об активности патологического процесса.
Мероприятия по лечению демиелинизирующих заболеваний бывают специфические и симптоматические. Новые исследования в медицине позволили добиться хороших успехов в специфических методах лечения. Бета-интерфероны считаются одними из самых эффективных препаратов: к ним относятся ребиф, бетаферон, аванекс. Клинические исследования бетаферона показали, что его применение снижает на 30% темпы прогрессирования заболевания, предотвращает развитие инвалидности и уменьшает частоту обострений.
Специалисты все чаще отдают предпочтение методу внутривенного введения иммуноглобулинов (биовен, сандоглобулин, веноглобулин). Таким образом проводится лечение обострений данного недуга. Более 20 лет назад была разработана новая, достаточно эффективная методика лечения демиелинизирующих заболеваний – иммунофильтрация ликвора. Сейчас ведутся исследования препаратов, действие которых направлено на прекращение процесса демиелинизации.
В качестве средств специфического лечения применяются кортикостероиды, плазмаферез, цитостатики. Также широко применяются ноотропы, нейропротекторы, аминокислоты, миорелаксанты.
Причины и факторы риска
О важности первых 2–3 месяцев внутриутробного развития ребёнка знают большинство будущим мам. Однако последний триместр беременности также таит в себе множество опасностей для полноценного роста и формирования головного мозга человека.
Снижение поступления кислорода к мозговым клеткам обусловлено метеорологическими условиями, провоцирующими спазмы сосудов.
Другие факторы неврологического заболевания:
- эндокринные нарушения у будущей матери – к примеру, диабет;
- анемия беременных;
- авитаминозы;
- внутриутробное инфицирование плода;
- обильные кровотечения в момент родовой деятельности;
- резкие колебания кровяного давления у малыша;
- ранняя острая дыхательная недостаточность у новорожденного.
Тем не менее, главной причиной лейкомаляций головного мозга остается глубокая недоношенность. Поэтому основной упор акушеры-гинекологи делают на своевременную профилактику преждевременных родов и внутриутробной кислородной недостаточности.
Почки и надпочечники
МРТ почек позволяет диагностировать следующие заболевания:
- аномалии развития,
- абсцессы почек,
- поликистоз (кисты в почках)
- гидронефроз,
- камни в почках,
- воспалительные заболевания (пиелонефрит, гломерулонефрит, туберкулез),
- оценка опухоли (к примеру, карцинома или переходно-клеточный рак),
- оценка при ксантогранулематозном пиелонефрите,
- оценка доброкачественных опухолей (к примеру, онкоцитома и ангиомиолипома);
Однако наибольшую ценность МР-исследование представляет в дифференциальной диагностике опухолей и кистозных образований почек.
МРТ позволяет выявить новообразования менее 2 см в диаметре, обнаружить метастазы в лимфатические узлы и опухолевые тромбы в сосудах почки.
Патология надпочечников часто выявляется случайно при выполнении МРТ забрюшинного пространства. Чаще всего удается диагностировать:
- доброкачественные;
- злокачественные опухоли, метастазы;
- произвести оценку причин гормонального дисбаланса.
Признаки доброкачественного новообразования надпочечников:
- округлая форма,
- ровный, четкий контур,
- структура однородная.
Признаки злокачественной опухоли надпочечников:
- неправильная форма,
- контур неровный, размытый,
- гетерогенная структура (отмечаются участки с различной интенсивностью сигнала)
Процесс формирования патологии
Для того чтобы понять, что такое ПВЛ и как с нею бороться, необходимо разобраться в механизме ее формирования. На фоне провоцирующих факторов в нервных клетках появляется патологический очаг – из-за кислородного голодания белое вещество органа отмирает. Полноценные нейроциты заменяются иными элементами, которые не способны выполнять те же функции.
Позже – через 7-14 суток на этом участке возникают перивентрикулярные кисты – полые или заполненные особой жидкостью. На завершающем этапе могут появляться рубцы на нервной ткани. Реже в боковых желудочках органа могут наблюдаться вторичные геморрагические инфаркты. В последующем пораженные участки полностью атрофируются.
Как правило, перивентриулярная лейкомаляция развивается в первые часы появления малыша на свет. Однако встречаются случаи, когда перивентрикулярный вариант патологии возникают позднее – до 5-7 суток от момента родов.
Поражение боковых желудочков головного мозга может происходить и внутриутробно – при беременности, сопровождающейся обострением пиелонефрита, гепатита. Для того чтобы этого избежать, женщине необходимо обращаться к наблюдающему за течением беременности врачу при первых же признаках ухудшения самочувствия.
Диагностика
Основной метод обнаружения очагов демиелинизации головного мозга – магнитно-резонансная томография. Она позволяет составить точную картину болезни. Введение контрастного вещества четче их очерчивает, позволяя выделить новые поражения белого вещества головного мозга.
Другие методы обследования включают пробы крови, исследование спинномозговой жидкости.
Симптомы и признаки болезни
Заподозрить, что лейкомаляция головного мозга у новорожденных появилась, затруднительно – признаки перивентрикулярной патологии разнообразны и крайне неспецифичны. Тем не менее, недостаток поступления кислорода к нервным клеткам не протекает вовсе бессимптомно. Основные клинические признаки перивентрикулярной лейкомаляции:
- чрезмерная возбудимость новорожденного – крикливость, избыточная хаотичность движений;
- склонность к судорожным состояниям;
- вялость мышечных рефлексов.
У глубоко недоношенных детей симптоматика намного грубее:
- колебание температуры тела;
- вялость;
- повышенная сонливость;
- снижение аппетита;
- нарушение сна;
- парезы/параличи конечностей;
- дыхательные расстройства;
- зрительные нарушения – косоглазие.
Специалисты подчеркивают – проявления перивентрикулярной формы заболевания после острого периода могут стихать. Этот период мнимого благополучия длится до 8-9 месяцев. И только к году лейкомаляция головного мозга дает о себе знать дефицитом нервной деятельности. О течение патологического процесса свидетельствуют:
- недостаточная прибавка в весе;
- медленный рост;
- отставание в освоении навыков;
- несоответствие интеллекта возрасту;
- задержка психоречевого развития;
- выраженная эмоциональная лабильность.
Желчный пузырь
В норме желчный пузырь имеет грушевидную форму с четкими контурами и однородным содержимым. Горизонтальный размер – менее 5см. Толщина стенки 1-3 мм. Ширина общего желчного протока менее 8 мм.
Наиболее полное представление о состоянии желчного пузыря дает бесконтрастная магнитно-резонансная холангиопанкреатография. МР-холангиография позволяет выявить камни в желчном пузыре и желчевыводящих путях, диагностировать стриктуры (сужения) желчных протоков, аномалии их развития.
На МР-изображениях свободная желчь имеет гиперинтенсивный признак, а камни отображаются в виде темных пятен (дефект заполнения).
Прогнозы и степень тяжести ПВЛ
Если женщине не удается доносить малыша до положенного срока – дети появляются на свет недоношенными. Родителям следует заранее подготовиться к правильному уходу за новорожденным.
Относительно благоприятным прогноз будет при легкой степени лейкомаляции головного мозга. В перивентрикулярной клинике преобладает дефицит внимания, а также гиперактивность – хаотичность движений конечностей. Тогда как моторное развитие – своевременность ползанья, ходьбы, переворотов сохраняется.
Специальные коррекционные мероприятия позволяют добиться компенсации расстройства, улучшить физическое и интеллектуальное развитие.
При среднетяжелом и тяжелом характере перивентрикулярной лейкомаляции малыш не будет соответствовать усредненным возрастным нормам – родителям следует быть к этому готовыми. Он позже начнет переворачиваться, присаживаться, ходить.
Затруднено и речевое развитие – слоги появятся позднее, предложения же будут практически недоступны. Иные проявления перивентрикулярной патологии:
- отсутствие естественного детского любопытства;
- болезненность и напряженность мышц конечностей;
- беспокойность, чрезмерная плаксивость;
- нарушение сна – прерывистость, частая путаность дня с ночью;
- грудное вскармливание затруднено – плохо выражен сосательный, а также глотательный рефлекс;
- отклонения в дательной системе – потребность в применении аппарата искусственного дыхания.
Тактика лечения
Поскольку очаги лейкомаляции подразумевают необратимую гибель нервных клеток, то каких-либо четких схем устранения подобных перивентрикулярных состояний не разработано. Специалисты придерживаются симптоматического подхода – лечение направлено на уменьшение выраженности негативных проявлений.
Перивентрикулярная лейкомаляция у недоношенных детей требует незамедлительного принятия мер по улучшению снабжения клеток кислородом. Для этого следует восстановить полноценный кровоток. Эффективные группы медикаментов:
- ноотропы – усиливают приток крови к нервным клеткам: Пирацетам;
- противосудорожные средства – Карбамазепин;
- витаминные комплексы;
- при высоком внутричерепном давлении – Диакарб;
- при повышенной плаксивости, нарушении сна – успокоительные лекарства на растительной основе, к примеру, Валериана, Мелисса.
Помимо медикаментозной терапии, врачи рекомендуют курсы лечебного массажа и физиотерапии. Обязательно проводятся коррекционные занятия с психологом, педагогами – для стимулирования памяти, мышления, внимания, а также речи.
При тяжелой степени перивентрикулярной болезни лечебные мероприятия будут проводиться в стационарных условиях – восстановление дыхательной, сердечнососудистой деятельности, компенсация внутричерепной гипертензии. В этом случае о благоприятном прогнозе речи уже вестись не будет.
Показания
Если другие методы исследования дали сомнительные результаты (КТ, УЗИ, рентген и пр.) или их выполнение невозможно, то томография позволяет дифференцировать различные состояния и болезни:
- Диагностика заболеваний печени и желчевыводящих путей;
- Желтуха любой этиологии;
- Внутренние кровотечения;
- Необъяснимая боль в животе;
- Увеличение печени и селезенки неизвестного генеза;
- Ишемические изменения в тканях;
- Полипы в желчном;
- Желчнокаменная болезнь и ее осложнения (камни в желчном пузыре);
- Камни в почках, песок в почках;
- Заболеваний поджелудочной железы (острый и хронический панкреатит);
- Врожденные аномалии органов или сосудов;
- Подозрение на опухоли печени, рак поджелудочной железы, почек, надпочечников, внеорганные образования;
- Дифференциальная диагностика объемных образований во внутренних органах, выявленных другими методами исследования;
- Оценка состояния селезенки при заболеваниях крови;
- Травмы живота;
- Выявление поражение лимфоузлов забрюшинного пространства;
- Доброкачественные образования — кисты, аденомы, полипы;
- Предоперационная подготовка;
- Послеоперационный контроль или выявление осложнений;
- Контроль эффективности лечения.
Обзорная МРТ брюшной полости оценивает структуру, размеры, расположение, форму, кровоснабжение органов, расположенных в ней.
Профилактика
Крепкое здоровье детей – это результат усилий их мам с первых дней, когда они узнали о своей беременности. Для того чтобы перивентрикулярная лейкомаляция не возникала, рекомендуется заранее принимать меры профилактики:
- соблюдать принципы здоровой жизни еще на этапе планирования беременности;
- придерживаться сбалансированного питания, с присутствием в рационе различных овощей и фруктов;
- отказаться от всех вредных привычек, особенно употребления табачной и алкогольной продукции;
- заранее пройти консультацию врача, сдать анализы на присутствие в организме скрытых инфекций;
- избегать тяжелых физических, психоэмоциональных нагрузок;
- укреплять защитные барьеры – принимать витаминные комплексы;
- хорошо высыпаться;
- свести к минимуму контакты с людьми, страдающими от заболеваний инфекционного характера.
Узнавшей о своей беременности женщине следует незамедлительно встать на учет к врачу, который будет ее наблюдать на всех этапах внутриутробного развития малыша. Профилактике различных патологий, в том числе и периветрикулярной лейкомаляции у новорожденных, специалистами системы здравоохранения уделяется огромное внимание – разработаны стандарты профилактических исследований у беременных.
Результаты
Что показывает МРТ брюшной полости и забрюшинного пространства? При обзорной томографии сканируются все внутренние органы, расположенные в брюшной полости и забрюшинно. Томография позволяет определить:
- строение органов, их размеры и расположение;
- аномалии развития;
- различные патологические изменения (воспаление, дистрофия, кистозное преобразование);
- доброкачественные новообразования
- первичные злокачественные опухоли и метастатическое поражение;
- нарушения кровообращения;
- поражение крупных сосудов (аорты, нижней полой вены);
- камни в желчного пузыре и почках.
Наиболее рационально использовать МРТ в качестве уточняющего метода исследования.
Что показывает МРТ с контрастом?
Кисты, гемангиомы, злокачественные опухоли на обычных МРТ снимках очень похожи между собой. Контрастирование применяется для отличия этих объемных образований. По особенностям заполнения их контрастом можно точно установить их природу.