Лейкоэнцефалопатия головного мозга — эта патология, при которой наблюдается поражение белого вещества, вызывающее слабоумие. Выделяют несколько нозологических форм, вызываемых различными причинами. Общим для них является наличие лейкоэнцефалопатии.
Спровоцировать заболевание могут:
- вирусы;
- сосудистые патологии;
- недостаточное снабжение головного мозга кислородом.
Другие названия заболевания: энцефалопатия, болезнь Бинсвангера. Впервые патология была описана в конце XIX веке немецким психиатром Отто Бинсвангером, который назвал ее в свою честь. Из этой статьи вы узнайте, что это такое, каковы причины болезни, как она проявляется, диагностируется и лечится.
Классификация
Различают несколько видов лейкоэнцефалопатии.
Мелкоочаговая
Это лейкоэнцефалопатия сосудистого генеза, которая представляет собой хроническую патологию, развивающуюся на фоне высокого давления. Другие названия: прогрессирующая сосудистая лейкоэнцефалопатия, субкортикальная атеросклеротическая энцефалопатия.
Одинаковые клинические проявления с мелкоочаговой лейкоэнцефалопатией имеет дисциркуляторная энцефалопатия — медленно прогрессирующее диффузное поражение сосудов головного мозга. Раньше эта болезнь была включена в МКБ-10, сейчас она в ней отсутствует.
Чаще всего мелкоочаговую лейкоэнцефалопатию диагностируют у мужчин старше 55 лет, у которых имеется генетическая предрасположенность к развитию этого заболевания.
В группу риска входят пациенты, страдающие такими патологиями, как:
- атеросклероз (холестериновые бляшки закупоривают просвет сосудов, в результате наблюдается нарушение кровоснабжения головного мозга);
- сахарный диабет (при этой патологии кровь сгущается, замедляется ее течение);
- врожденные и приобретенные патологии позвоночника, при которых наблюдается ухудшения кровоснабжения мозга;
- ожирение;
- алкоголизм;
- никотиновая зависимость.
Также к развитию патологии приводят погрешности в диете и гиподинамичный образ жизни.
Прогрессирующая мультифокальная лейкоэнцефалопатия
Это самая опасная форма развития заболевания, которая нередко становится причиной летального исхода. Патология имеет вирусную природу.
Ее возбудителем является полиомавирус человека 2. Этот вирус наблюдается у 80% человеческой популяции, но заболевание развивается у пациентов с первичным и вторичным иммунодефицитом. У них вирусы, попадая в организм, еще сильнее ослабляют иммунную систему.
Прогрессирующая многоочаговая лейкоэнцефалопатия диагностируется у 5% ВИЧ-положительных пациентов и у половины больных СПИДом. Раньше прогрессирующая мультифокальная лейкоэнцефалопатия встречалось еще чаще, но благодаря ВААРТ распространенность этой формы снизилась. Клиническая картина патологии полиморфна
.
Заболевание проявляется такими симптомами, как:
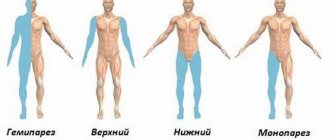
- периферические парезы и параличи;
- односторонняя гемианопсия;
- синдром оглушения сознания;
- дефект личности;
- поражение ЧМН;
- экстрапирамидные синдромы.
Нарушения со стороны ЦНС могут существенно варьировать от небольшой дисфункции до тяжелой степени слабоумия. Могут наблюдаться нарушения речи, полная потеря зрения. Зачастую у пациентов развиваются тяжелые нарушения со стороны опорно-двигательного аппарата, которые становятся причиной потери работоспособности и инвалидизации.
В группу риска входят следующие категории граждан:
- пациенты с ВИЧ и СПИДом;
- получающие лечение моноклональными антителами (их назначают при аутоиммунных заболеваниях, онкологических болезнях);
- перенесшие пересадку внутренних органов и принимающие иммунодепрессанты с целью предупредить их отторжение;
- страдающие злокачественной гранулемой.
Перивентрикулярная (очаговая) форма
Развивается в результате хронического кислородного голодания и нарушения кровоснабжения головного мозга. Ишемические участки расположены не только в белом, но и сером веществе.
Обычно патологические очаги локализованы в мозжечке, мозговом стволе и лобной части коры больших полушарий. Все эти структуры мозга отвечают за движение, поэтому при развитии такой формы патологии наблюдаются двигательные расстройства.
Это форма лейкоэнцефалопатии развивается у детей, у которых есть патологии, сопровождающиеся гипоксией при родоразрешении и в течение нескольких дней после появления на свет. Также данную патологию называют “перивентрикулярная лейкомаляция”, как правило, она провоцирует ДЦП.
Лейкоэнцефалопатия с исчезающим белым веществом
Она диагностируется у детей. Первые симптомы патологии наблюдаются у пациентов в возрасте от 2 до 6 лет. Появляется она из-за генной мутации.
У пациентов отмечается:
- нарушение координации движения связанное с поражением мозжечка;
- парез рук и ног;
- ухудшение памяти, снижение умственной работоспособности и другие когнитивные нарушения;
- атрофия зрительного нерва;
- эпилептические приступы.
У детей до года наблюдается проблемы со вскармливанием, рвота, высокая температура, психическое отставание, чрезмерная возбудимость, повышенный тонус мышц рук и ног, судороги, ночное апноэ, кома.
Купить онлайн
Прогрессирующая мультифокальная лейкоэнцефалопатия (ПМЛ) — это редкое прогрессирующее демиелинизирующее заболевание центральной нервной системы (ЦНС), вызванное реактивацией существующего в латентном состоянии папова вируса (JC-вируса) при иммунодефицитных состояниях [8].
Первое описание двух случаев, похожих на ПМЛ, было сделано в 1930 г. J. Halervorden. Термин ПМЛ был введен в 1958 г. K. Astrom и соавт. [2], которые выделили ПМЛ в самостоятельное заболевание. Первые случаи ПМЛ были описаны ими при лимфопролиферативных заболеваниях — хроническом лимфолейкозе, ходжкинской лимфоме. Предположение о вирусной этиологии заболевания впервые было высказано в работах [23] после идентификации внутриядерных включений в олигодендроглиоцитах.
Вирусная этиология ПМЛ была установлена в 1971 г., когда из мозга больного J. Cunningham был выделен вирус, получивший название по имени этого исследователя — JC-вирус [21]. В 1984 г. было установлено, что JC-вирус является ДНК-содержащим вирусом семейства папова вирусов [10].
В развитии эпидемиологических исследований при ПМЛ можно выделить 4 этапа. До 80-х годов ПМЛ являлась редким заболеванием; заболеваемость составляла 1:1 000 000 человек. С 1958 по 1984 г. всего описано 230 случаев ПМЛ. До эпидемии СПИДа 80% случаев ПМЛ было связано с лимфопролиферативными заболеваниями, ходжкинской лимфомой, тяжелыми формами туберкулеза. С начала 90-х годов (1990-1996), в связи с ростом ВИЧ-инфекции, заболеваемость ПМЛ выросла в 5 раз и в настоящее время составляет 1:200 000 человек в популяции [22]. При этом среди ВИЧ-инфицированных встречаемость ПМЛ до применения высокоактивной антиретровирусной терапии (ВААРТ) составляет 3,3:1000. С внедрением ВААРТ заболеваемость ПМЛ снизилась в 2,5 раза и составила 1,3 на 1000 ВИЧ-инфицированных [9]. С 2005 г. все чаще стали регистрировать случаи ПМЛ у не ВИЧ-инфицированных больных с аутоиммунными заболеваниями, после трансплантации органов, с рассеянным склерозом в результате применения новых методов агрессивной иммуносупрессии (глюкокортикостероиды, пуриновые аналоги — флударибин, кладрибин, азатиоприн, алкилирующие соединения — циклофосфамид, кармустин, декарбазин, моноклональные антитела). Заболеваемость ПМЛ у этих пациентов колеблется от 1:1000 до 1:10 000 [11, 15, 16].
Согласно современным эпидемиологическим данным, к основным состояниям, вызывающим ПМЛ, относятся: ВИЧ/СПИД в 80% случаев, лимфомиелопролиферативные заболевания и злокачественные опухоли в 13% случаев, трансплантация органов и тканей в 5% случаев и аутоиммунные воспалительные заболевания, в том числе системная красная волчанка, склеродермия, ревматоидный артрит, дерматомиозит, которые составляют 2% случаев.
До настоящего времени механизм заражения JC-вирусом неизвестен. Предполагают как воздушно-капельный, так и фекально-оральный пути заражения. Асимптомное инфицирование происходит в ранний период жизни, при этом персистенция вируса наблюдается в CD34 стволовых клетках костного мозга, лимфоидных органах и эпителиальных клетках почек, куда JC-вирус попадает из лимфоцитов периферической крови и миндалин.
В то же время у детей старше 11 лет в крови выявляются специфические антитела к JC-вирусу в 50% случаев, у лиц старше 30 лет — в 80%. У здоровых лиц JC-вирус не вызывает развития ПМЛ, хотя периодически он выделяется методом полимеразной цепной реакции (ПЦР) у 30% — в моче и у 39% — в ткани миндалин [4].
При иммунодефицитном состоянии происходит реактивация JC-вируса с попаданием его в кровь и далее в ЦНС.
В настоящее время доказано, что существуют различные изоформы JC-вируса в гемопоэтической и мочевыделительной системах. При ПМЛ в мозге идентифицирована изоформа JC-вируса, гомологичная вирусу, выделенному из костного мозга, но не из мочи и почечного эпителия.
Генетические исследования позволили идентифицировать ряд изменений регуляторного участка вирусного генома и точковые мутации VPI белка JC-вируса, выделенного из мозга больных ПМЛ в отличие от здоровых лиц [27, 29].
Геном JC-вируса содержит некодируемый контролирующий участок (noncoding control region NCCR). У пациентов ПМЛ этот участок реорганизуется в специфическую форму «Mad», которая идентифицирована только в их мозге и цереброспинальной жидкости (ЦСЖ). Предполагают, что в условиях иммуносупрессии JC-вирус реактивируется на периферии, а затем происходит его генетическая перестройка из NCCRArch (классическая форма) в NCCRMad-генотип, что делает эту форму инвазивной для ЦНС. Именно NCCRMad JC-вирус способен проникать через гематоэнцефалический барьер (ГЭБ), инфицировать олигодендроглиоцит и реактивироваться в этой клетке, вызывая в дальнейшем ее гибель.
Генетические модификации усиливают аффинность и специфичность JC-вируса к клеточным рецепторам, повышая его вирулентность и трансмиссивность.
Ключевым звеном в предотвращении реактивации вируса и развития ПМЛ является состояние Т-клеточного иммунитета, содержание CD4+ Т-клеток и цитотоксичных CD8+ Т-клеток [18].
Это подтверждается развитием ПМЛ только при иммунодефицитных состояниях, а также прямой связью между содержанием CD4+ и CD8+ Т-клеток и прогнозом у ВИЧ-инфицированных больных ПМЛ. Известно, что глубокая иммуносупрессия (не менее 6 мес) предшествует реактивации JC-вируса.
Основными факторами риска развития ПМЛ являются длительная иммуносупрессия и угнетение Т-клеточного звена иммунитета. Учитывая, что большинство больных ПМЛ (85%) являются
ВИЧ-инфицированными, у этих больных основным предрасполагающим фактором является значительное снижение числа CD4+ Т-клеток (менее 200 клеток/мкл).
При других состояниях количество CD4+ Т-клеток может быть различно, при этом уровень их определяет темп развития ПМЛ. Так, при ПМЛ, вызванной применением ритуксимаба, установлено, что уровень CD4+ Т-клеток определяет интервал между последней дозой препарата и манифестацией клинических проявлений ПМЛ. При содержании CD4+ Т-клеток менее 500 клеток/мкл и выраженном снижении иммуноглобулинов IgG ПМЛ у больных, получающих ритуксимаб, развивается менее чем через 3 мес после последнего введения препарата. При уровне CD4+ Т-клеток более 500 клеток/мкл этот период несколько продолжительнее (в среднем 17 мес).
Уровень CD4+ Т-клеток и снижение индекса CD4+ Т-клеток/CD8+ Т-клеток влияет не только на темп развития ПМЛ, но и на выживаемость. Смертность от ПМЛ у больных с низким уровнем CD4 +Т-клеток (менее 500/мкл) на фоне лечения ритуксимабом составляет 100%, тогда как у остальных больных — 84%.
In vitro
JC-вирус способен инфицировать олигодендроциты, астроциты, моноциты, В-лимфоциты, Т-лимфоциты, клетки предшественники гемопоэтических клеток в костном мозге. В настоящее время превалирует мнение о реактивации вируса на периферии и проникновении его через ГЭБ в ткани мозга.
В ЦНС основной мишенью для JC-вируса являются олигодендроциты, с которыми он связывается через серотониновый 5-гидрокситриптамин-2А рецептор на поверхности глиальных клеток. Эти же рецепторы экспрессируются астроцитами, В-клетками, почечным эпителием. JC-вирус вызывает лизис миелинобразующей клетки и, как следствие, массивную демиелинизацию мозговой ткани.
Основными патоморфологическими признаками ПМЛ являются множественные очаги демиелинизации, вызванные гибелью олигодендроцитов, наибольшее число их встречается в полушариях большого мозга, мозговом стволе и мозжечке. Воспалительные изменения в головном мозге практически отсутствуют.
Гистологически при ПМЛ выявляются следующие изменения: измененные олигодендроциты с увеличенными ядрами и внутриядерными вирусными включениями; пролиферация астроцитов с образованием гигантских причудливой формы клеток с гиперхроматическими ядрами; множественные очаги демиелинизации с образованием полостей в них; иногда наблюдаются также изменения в нервных клетках мозжечка с вирусными внутриядерными включениями.
Заболевание характеризуется подострым (несколько дней) или постепенным (несколько недель) развитием неврологической и психопатологической симптоматики. Характерно отсутствие общеинфекционных, общемозговых и менингеальных симптомов. Наиболее часто при дебюте заболевания появляются двигательные нарушения (гемипарезы, мозжечковая атаксия), нарушения зрения (гемианопсии), нарушения высших корковых функций (афазия), психические расстройства.
В конечной стадии заболевания наблюдаются глубокая деменция, кома и гибель больного. Течение вариабельно, летальный исход наступает в течение 6-12 мес.
Клиническая картина заболевания, появление и прогрессирование неврологической и психической симптоматики у иммунодефицитного больного заставляют заподозрить ПМЛ. Наибольшие диагностические трудности возникают при СПИДе, когда клиника и МРТ-признаки сходны при ПМЛ и ВИЧ-ассоциированной энцефалопатии [17].
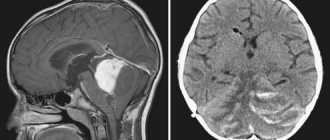
МРТ головного мозга является необходимым методом диагностики при подозрении на ПМЛ. МРТ-картина при подозрении на ПМЛ характеризуется мультифокальными очагами высокой интенсивности сигнала с нечеткими границами на Т2-взвешенных изображениях в подкорковом белом веществе. Чаще поражается белое вещество теменных и затылочных долей, однако очаги могут наблюдаться в любых отдела мозга, включая мозжечок и ствол [1].
В начале заболевания выявляется несколько очагов, по мере прогрессирования процесса отмечается нарастание количества сливных очагов. Очень редко наблюдается незначительный масс-эффект, и в этих случаях их трудно отличить от глиомы. Контрастное усиление отсутствует в результате малой выраженности воспаления. Однако у 5-15% больных отмечается контрастирование по периферии очагов. У 50% больных поражается также и серое вещество [6]. Задняя черепная ямка поражается у 48% больных. Спинной мозг вовлекается крайне редко. Поражение зрительных нервов при ПМЛ не наблюдается.
JC-вирус не вызывает общевоспалительной реакции, в связи с чем изменения в крови и ЦСЖ неспецифичны и не коррелируют с наличием в ЦСЖ JC-вируса. Состав ЦСЖ при ПМЛ у 71% больных не отличается от нормы. У 29% имеется легкое повышение белка (40-80 мг/мл), у 6% — небольшой плейоцитоз (до 16 клеток в 1 мл).
Диагностика ПМЛ в настоящее время основывается на клинических проявлениях заболевания, данных МРТ и результатах исследования ЦСЖ и мозга больных на наличие JC-вируса. Согласно современной классификации, вероятный диагноз может быть выставлен при наличии характерных клинических и нейровизуализационных проявлений при отсутствии JC-вируса в ЦСЖ и мозговой ткани. Лабораторно подтвержденный диагноз устанавливается при наличии ДНК JC-вируса в ЦСЖ больного по данным ПЦР. Гистологически подтвержденный диагноз ПМЛ устанавливается в случае определения JC-вируса методом ПЦР в биопсийном материале мозга больного.
Дифференциальный диагноз ПМЛ должен проводиться со СПИД-деменцией или ВИЧ-энцефалопатией, с оппортунистическими инфекциями ЦНС (энцефалиты цитомегаловирусной, токсоплазменной и грибковой этиологии), а также лимфомой головного мозга. Наибольшие трудности вызывает дифференциальная диагностика с ВИЧ-энцефалопатией, которая может не отличаться ни по клиническим, ни по нейровизуализационным признакам от ПМЛ. В данных случаях только выявление JC-вируса в ЦСЖ и биоптатах головного мозга позволяет установить диагноз [18].
Развитие ПМЛ у больных с аутоиммунными заболеваниями и рассеянным склерозом, получавших терапию моноклональными антителами (ритуксимаб, натализумаб), делает необходимым учитывать возможность развития ПМЛ у этих больных.
Появление нехарактерных клинических симптомов (когнитивные нарушения, афазия, гемианопсия, психические расстройства), прогрессирующее течение ранее ремиттирующего заболевания, появление новых очагов на МРТ, не накапливающих контрастное вещество, являются основаниями предположить наличие ПМЛ у этих пациентов. Основным подтверждением является наличие JC-вируса в ЦСЖ. При отрицательном результате необходимо повторять исследование ЦСЖ каждые 4 нед. Биопсия головного мозга проводится в редких случаях при отсутствии JC-вируса в ЦСЖ при повторных исследованиях.
Дифференциальный диагноз должен проводиться также с токсической лейкоэнцефалопатией, вызванной действием цитостатиков, и различными инфекциями ЦНС (herpes simplex
, вирус CMV,
varicella zoster, criptocoсcus, aspergillus
). В отличие от вышеназванных инфекций, при ПМЛ не встречается общеинфекционных и менингеальных симптомов в связи с отсутствием воспалительной реакции как в ЦНС, так и на периферии.
Исследования последних лет показали, что использование специфических моноклональных антител при рассеянном склерозе, аутоиммунных и лимфопролиферативных заболеваниях повышает риск развития ПМЛ среди пациентов, которые получают эти препараты. К моноклональным антителам относятся такие препараты, как ритуксимаб, натализумаб, инфликсимаб, этанерцепт и др. Ритуксимаб является препаратом моноклональных антител против CD20 предшественников В-лимфоцитов и зрелых В-лимфоцитов. Разрешен к применению при клеточной неходжкинской лимфоме, резистентном ревматоидном артрите. В 2006 г. одобрен FDA для лечения системной краской волчанки. В настоящее время для контроля за действием ритуксимаба и выявления побочных эффектов препарата действует специальный проект (RADAR Research on Advers Drag Events and Report) при участии вирусологов, онкологов, неврологов и других специалистов [3]. Риск развития ПМЛ у больных, получающих ритуксимаб, составляет 1:8000 [16].
На сегодняшний день отмечено 270 случаев развития ПМЛ при применении ритуксимаба; смертность среди этих больных составляет 90%.
Натализумаб — препарат моноклональных антител к α-4 субъединице α-4β1 и α-4β7 интегринов, экспрессирующихся лейкоцитами и являющихся молекулами адгезии; используется в клинической практике с 1999 г. при рассеянном склерозе, ревматоидном артрите, болезни Крона. В связи с развитием 3 случаев ПМЛ у 2 больных рассеянным склерозом и 1 больного болезнью Крона с 28 февраля 2005 г. было приостановлено его применение.
Предполагают несколько механизмов развития ПМЛ при лечении натализумабом: снижение иммунного лейкоцитарного ответа и реактивация JC-вируса; стимуляция высвобождения JC-вируса из костного мозга и незрелых лейкоцитов [14, 26]. Была разработана и утверждена специальная программа для уменьшения риска развития ПМЛ у больных, получающих натализумаб (Risk Minimization Action Plan — Risk MAP). В связи с этим в США действует программа Tysabri Outreach Unified Committee to Health — TOUCH [15, 28].
Препарат был вновь разрешен к применению в мае 2006 г. с определенными ограничениями. К январю 2012 г. зарегистрировано 207 случаев ПМЛ у пациентов, получающих натализумаб. Риск развития данного осложнения у этих больных составляет 1:1000. При этом в США зарегистрировано 79 случаев развития ПМЛ, в странах Евросоюза — 118 случаев, в других странах — 10 случаев ПМЛ. Смертность в случае развития ПМЛ при этом составляет 21%.
К февралю 2012 г. умерли 44 (21%) пациента. Большинство смертельных исходов отмечено через 2-3 мес после выявления ПМЛ.
В апреле 2012 г. был описан 1 случай ПМЛ у больного РС, получающего финголимод и в анамнезе терапию натализумабом [9].
Предшествующее назначение иммуносупрессивной терапии, наличие повышенного титра антител к JC-вирусу повышают риск развития ПМЛ у пациентов, получающих иммуносупрессивную терапию длительностью более 24 мес.
В настоящее время разработаны критерии включения и исключения при применении натализумаба у больных с РС [5, 12]. Индивидуальных критериев назначения моноклональных антител после той или иной терапии не разработано [13].
На сегодняшний день эффективного лечения ПМЛ не существует [8]. Используют различные классы лекарственных препаратов: противовирусные средства, цитостатики, антагонисты серотониновых рецепторов, а также трансплантацию стволовых клеток костного мозга [19, 25].
ВААРТ у ВИЧ-инфицированных больных — это мультикомплексная терапия, состоящая из нуклеозидного ингибитора обратной транскриптазы (тимозид, зидовудин), ненуклеозидного ингибитора обратной транскриптазы (делавердин, рескриптор и др.), ингибитора протеаз (санвиновир, инвираза и др.). Лечение ВИЧ и ПМЛ с использованием ВААРТ увеличило выживаемость больных с 3-6 мес до 19,6 мес, снизило заболеваемость ПМЛ и другими оппортунистическими инфекциями ВИЧ-инфицированных больных. В то же время у некоторых больных ВААРТ приводит к манифестации ПМЛ или ухудшению течения ПМЛ, что обусловлено развитием так называемого иммунного реконструктивного воспалительного синдрома (IRIS — immune reconstrictution inflammatory syndrome). Предполагают, что активация инфекции связана с изменением баланса CD8+/CD4+ Т-клеток [20].
Наиболее часто при ПМЛ у не ВИЧ-инфицированных больных используют противовирусные препараты цидофир (вистид), интерферон-альфа, интерлейкин-2.
Стабилизация процесса отмечалась у нескольких больных ПМЛ при лечении цитарабином (известном также как цитозар — ингибитор ДНК полимеразы и репликации вируса).
Современным направлением в лечении ПМЛ является использование препаратов блокаторов 5-гидрокситриптамина-2а серотониновых рецепторов, необходимых для проникновения JC-вируса в клетку.
Оказались способны блокировать JC-вирусную репликацию в олигодендроцитах в ЦНС атипичные антипсихотические средста (рисперидон, оланзапин, зипразидон), которые не только могут приводить к регрессу когнитивных нарушений, но и повышать выживаемость больных.
Наиболее эффективным терапевтическим подходом является восстановление клеточного иммунитета у больных в результате либо снижения дозы иммуносупрессоров, либо их отмены (за исключением состояний после трансплантации органов). Подтверждением этому являются единичные случаи регресса симптоматики и выздоровления больных после отмены цитостатиков [7, 24].
Использование плазмафереза у больных РС, получающих натализумаб, позволило снизить смертность до 21%. По существующим рекомендациям, проведение 5 процедур плазмафереза в течение
10 дней приводит к быстрому восстановлению иммунокомпетентности в головном мозге и способствует своевременной стабилизации состояния пациентов с ПМЛ [28].
Клиническая картина
Обычно признаки лейкоэнцефалопатии нарастают постепенно. В начале болезни пациент может быть рассеянным, неловким, безразличным к происходящему. Он становится слезливым, с трудом произносит сложные слова, у него падает умственная работоспособность.
Со временем присоединяются проблемы со сном, повышается мышечный тонус, больной становится раздражительным, у него наблюдается непроизвольное движение глаз, появляется шум в ушах.
Если не начать лечить лейкоэнцефалопатию на этой стадии, но она прогрессирует: возникают психоневроз, выраженное слабоумие и судороги.
Главными симптомами заболевания являются следующие отклонения:
- двигательные расстройства, которые проявляются нарушением координации движения, слабостью в руках и ногах;
- может быть односторонний паралич рук или ног;
- речевые и зрительные расстройства (скотома, гемианопсия);
- онемение различных частей тела;
- нарушение глотания;
- недержание мочи;
- эпилептический приступ;
- ослабление интеллекта и небольшое слабоумие;
- тошнота;
- головные боли.
Все признаки поражения нервной системы прогрессируют очень быстро. У пациента может отмечаться ложный бульбарный паралич, а также паркинсонический синдром, который проявляется нарушением походки, письма, дрожанием тела.
Почти у каждого пациента наблюдается ослабление памяти и интеллекта, неустойчивость при изменении положения тела или ходьбе.
Обычно люди не понимают, что больны, и поэтому к доктору их зачастую приводят родственники.
Поздняя симптоматика
Мультифокальная лейкоэнцефалопатия в 70-80% случаев заявляет о себе ощущением постоянной слабости – на протяжении всего дня, даже в утренние часы после сна. Для большинства случаев будет характерно поражение зрительной системы – значительное ухудшение зрения, вплоть до слепоты.
Основные клинические проявления развернутой стадии мультифокальной прогрессирующей лейкоэнцефалопатии:
- мышечный тремор – непроизвольное сокращение мышечных волокон в разных частях тела, чаще в нижних и верхних конечностях,
- чувствительность покровных тканей искажена – больной хуже воспринимает температурные, механические воздействия,
- изменение походки – ее шаткость, неуверенность,
- когнитивные нарушения – ослабление памяти, внимания,
- судороги – поначалу в одной половине тела, затем распространенные,
- сознание – остается ясным, но видны признаки деменции, что проявляется в спутанности ориентирования в происходящих событиях, окружающем мире, личности.
У трети больных будут появляться психические отклонения – подозрительность, галлюцинации, агрессивность, которые будут постепенно прогрессировать. Постепенно нарастает выраженность парезов и параличей – вплоть до полной парализации. Человекстановится глубоким инвалидом и требует постоянного постороннего ухода.
Диагностика
Чтобы поставить диагноз «лейкоэнцефалопатия», врач назначит комплексное обследование. Нужны будут:
- осмотр невролога;
- общий анализ крови;
- анализ крови на содержания наркотических, психотропных средств и алкоголя;
- магнитно-резонансная и компьютерная томография, которые позволяют выявить патологические очаги в головном мозге;
- электроэнцефалография головного мозга, которая покажет снижение его активности;
- ультразвуковая допплерография, которая позволяет выявить нарушение циркуляции крови по сосудам;
- ПЦР, позволяющий выявить ДНК-возбудителя в головном мозге;
- биопсия головного мозга;
- спинномозговая пункция, которая показывает повышенную концентрацию белка в спинномозговой жидкости.
В случае если врач подозревает, что в основе лейкоэнцефалопатии лежит вирусная инфекция, он назначает пациенту электронную микроскопию, которая позволит выявить в тканях головного мозга частицы возбудителя.
С помощью иммуноцитохимиеского анализа удается обнаружить антигены микроорганизма. В спинномозговой жидкости при таком течении заболевания наблюдается лимфоцитарный плеоцитоз.
Также помогают в постановке диагноза тесты на психологическое состояние, память, координацию движения.
Дифференциальная диагностика проводится с такими заболеваниями, как:
- токсоплазмоз;
- криптококкоз;
- ВИЧ-деменция;
- лейкодистрофия;
- лимфома центральной нервной системы;
- подострый склерозирующий панэнцефалит;
- рассеянный склероз.
Терапия
Лейкоэнцефалопатия относится к неизлечимым заболеваниям. Но обязательно нужно обращаться в больницу для подбора медикаментозного лечения. Цель терапии — замедлить прогрессирование заболевания и активировать функции головного мозга.
Лечение лейкоэнцефалопатии — комплексное, симптоматическое и этиотропное. В каждом конкретном случае оно подбирается индивидуально
.
Врач может прописать следующие медикаменты:
- лекарства, улучшающее мозговое кровообращение (Винпоцетин, Актовегин, Трентал);
- нейрометаболические стимуляторы (Фезам, Пантокальцин, Луцетам, Церебролизин);
- (Стугерон, Курантил, Зилт);
- поливитамины, в состав которых входят витамины группы В, ретинол и токоферол;
- адаптогены, такие как экстракт алоэ, стекловидное тело;
- глюкокортикостероиды, которые помогают купировать воспалительный процесс (Преднизолон, Дексаметазон);
- антидепрессанты (Флуоксетин);
- антикоагулянты, позволяющие снизить риск тромбозов (Гепарин, Варфарин);
- при вирусной природе заболевания назначаются Зовиракс, Циклоферон, Виферон.
Дополнительно показано:
- физиолечение;
- рефлексотерапия;
- аккупунктура;
- дыхательная гимнастика;
- гомеопатия;
- фитотерапия;
- массаж воротниковой зоны;
- мануальная терапия.
Трудность терапии заключается в том, что многие противовирусные и противовоспалительные препараты не проникают через ГЭБ, следовательно, не оказывают воздействия на патологические очаги.
Эффективная поддерживающая терапия
Эффективных препаратов от лейкоэнцефалопатии, к сожалению, до сих пор нет. Любой из типов болезни постепенно прогрессирует и остановить этот процесс полностью не удастся.
Терапевтические курсы, назначенные неврологом, призваны поддерживать состояние пациента. Цель такого лечения: замедление прогрессирования болезни, нивелирование симптомокомплекса и восстановление интеллектуальных способностей (адаптогены, транквилизаторы, ГКС, ангиопротекторы и так далее). Кроме того, для предотвращения каких-либо воспалительных процессов применяются кортикостероиды, а при наличии ВИЧ — антиретровирусные средства.
Самостоятельно принимать лекарства против лейкоэнцефалопатии запрещается, так как дозы подбираются индивидуально.
Прогноз при лейкоэнцефалопатии
В настоящее время патология неизлечима и всегда заканчивается летальным исходом. Сколько живут с лейкоэнцефалопатией, зависит от того, была ли вовремя начата противовирусная терапия.
Когда лечение не проводится совсем, продолжительность жизни пациента не превышает полугода с момента выявления нарушения структур мозга.
При проведении антивирусной терапии продолжительность жизни увеличивается до 1-1,5 лет.
Были отмечены случаи острого течения патологии, которые заканчивались гибелью пациента через месяц после ее начала.
Прогрессирующая мультифокальная лейкоэнцефалопатия
Прогрессирующая мультифокальная лейкоэнцефалопатия
— редкое демиелинизирующее заболевание, обусловленное реактивацией находящегося в организме большинства людей вируса JC.
Патология возникает на фоне угнетения иммунитета у больных СПИДом, гемобластозами, наследственными иммунодефицитами, у пациентов, получающих иммуносупрессивную терапию.
Диагностика базируется на клинических данных, результатах томографии головного мозга, ПЦР-исследования ликвора на вирусную ДНК, гистологии церебральных биоптатов. Специфическая терапия не разработана.
Прогрессирующая мультифокальная лейкоэнцефалопатия (ПМЛ) ассоциирована с JC-вирусом (JCV), возникает у иммунокомпрометированных пациентов, 85% из которых составляют ВИЧ-инфицированные.
Заболевание относится к оппортунистическим инфекциям, носителями вируса являются 90% человечества. До 90-х годов ХХ века заболеваемость ПМЛ не превышала 1 случая на 100 тыс. населения. С ростом числа больных СПИДом этот показатель увеличился до 1 на 20 тыс. человек.
Сегодня прогрессирующая лейкоэнцефалопатия наблюдается у 5% больных СПИДом. Некоторые авторы сообщают о снижении заболеваемости за последнее десятилетие в связи с успешным применением антиретровирусной терапии.
Одновременно отмечается увеличение распространённости ПМЛ среди лиц с аутоиммунными заболеваниями, что обусловлено использованием в их лечении агрессивной иммунотерапии.
Прогноз и профилактика
Прогрессирующая мультифокальная лейкоэнцефалопатия отличается неуклонно усугубляющимся течением с исходом в кому. Продолжительность жизни варьирует от 1 мес. (острая форма) до 10-12 мес. с момента заболевания.
Профилактика подразумевает меры предупреждения инфицирования ВИЧ, осторожное проведение терапии аутоиммунных заболеваний, мониторинг неврологической симптоматики у больных, получающих лечение моноклональными препаратами.
Источник: https://www.krasotaimedicina.ru/diseases/zabolevanija_neurology/progressive-multifocal-leukoencephalopathy
Профилактика
Специфической профилактики лейкоэнцефалопатии не существует.
Чтобы снизить риск развития патологии, нужно соблюдать следующие правила:
- укреплять свой иммунитет путем закаливания и приема витаминно-минеральных комплексов;
- нормализовать свой вес;
- вести активный образ жизни;
- регулярно бывать на свежем воздухе;
- отказаться от употребления наркотиков и алкоголя;
- бросит курить;
- избегать случайных половых контактов;
- при случайной интимной близости пользоваться презервативом;
- сбалансировано питаться, в рационе должны преобладать овощи и фрукты;
- научиться правильно справляться со стрессами;
- выделять достаточно времени для отдыха;
- избегать чрезмерных физических нагрузок;
- при выявлении сахарного диабета, атеросклероза, артериальной гипертензии принимать медикаменты, назначенные врачом с целью компенсации болезни.
Все эти меры позволят свести к минимуму риск развития лейкоэнцефалопатии. Если заболевание все-таки возникло, нужно как можно быстрее обратиться за медицинской помощью и начать лечение, которое поможет увеличить продолжительность жизни.
Цереброваскулярная болезнь на ранних стадиях проявляется снижением работоспособности, повышенной утомляемостью, снижением фона настроения, нарушениями сна, когда больной просыпается среди ночи, а затем не может заснуть. Затем присоединяются симптомы когнитивных нарушений, т.е. снижается память, замедляется мышление, затрудняется устный счет, появляется излишняя суетливость. В дальнейшем присоединяются упорные головные боли, шум в ушах, головокружение. Периодически развиваются мозговые кризы, которые протекают с грубым нарушением функций головного мозга и проявляются развитием слабости в конечностях с одной стороны, нарушениями речи, чувствительности, зрения. Если подобные симптомы проходят в течение 48 часов, то говорят о преходящем нарушении мозгового кровообращения. Если же симптомы сохраняются дольше, то это — инсульт. В этом случае грубые нарушения функции нервной системы могут сохраняться до конца жизни, инвалидизируя больного. Инсульт может быть ишемическим, в случае закрытия просвета сосуда атеросклеротической бляшкой или тромбом, или геморрагическим, когда происходит нарушение целостности сосудистой стенки и происходит кровоизлияние в мозг.
Лейкоэнцефалопатия — это хроническая болезнь, которая имеет способность к прогрессированию, и обусловленная разрушением клеток белого вещества отделов головного мозга. Данная патология приводит к слабоумию у старых людей, или же к деменции.
В 1894 году медик Бинсвангер подробно описал разрушительное действие лейкоэнцефалопатии.
Данная патология имеет название — заболевание энцефалопатия Бинсвангера. В современной медицине все чаще ставят диагноз ПМЛ (прогрессивная мультифокальная патология) — данная лейкоэнцефалопатия имеет этиологию вируса.
Причины и провоцирующие факторы
Возбудителем мультифокальной прогрессирующей лейкоэнцефалопатии является полиомавирус JC. Он распространен повсеместно – многие люди, даже сами не зная того, являются его здоровыми носителями. Инфицирование происходит двумя путями – капельно-воздушным, а также алиментарным (через рот).
На протяжении жизни вирус находится в скрытом состоянии во внутренних структурах организма человека – в почках, селезенке либо костном мозге. Активация вирусных элементов происходит из-за резкого снижения защитных барьеров организма. Особую подгруппу риска по появлению мультифокальной патологии составляют:
- ВИЧ-инфекция – протекает с угнетением клеточного иммунитета,
- гемобластозы – раковые поражения клеток крови приводят к формированию состояния иммунодефицита,
- аутоиммунные заболевания – на фоне активного иммуноугнетающего лечения, применяемого, к примеру, для терапии красной волчанки либо склеродермии,
- наследственные болезни – протекающие с иммунодефицитом,
- иммуносупрессии из-за трансплантации органов,
- вторичные иммунодефициты как результат проведения химиотерапии при различных онкологических болезнях.
Крайне редко мультифокальная лейкоэнцефалопатия является результатом приема человеком токсичных медицинских препаратов без назначения врача.
Лейкоэнцефалопатия головного мозга — что это такое?
Разрушительная гибель клеток в нервной системе головного мозга, которая спровоцирована гипоксией от недостаточного кровотока в орган приводит к — микроангиопатия. Заболевание лейкоареоз, а также патология инфаркты лакунарного типа изменяют структуру клеток белого вещества.
Данные изменения — это последствия плохой циркуляции кровотока в органе.
Проявления лейкоэнцефалопатии связаны с тяжестью заболевания, и симптоматика зависит от типа патологии. Подкорковый тип очень часто связан с лобными разрушениями, и выявляется в эпилептических припадках.
Патология имеет хроническую форму прогресса со своими рецидивами. Страдают от лейкоэнцефалопатии люди пожилого возраста, но нередки случаи постановки данного диагноза у более молодых пациентов.
Основные причины диффузии головного мозга:
- Недостаточность в головном мозге кровотока (провокатор ишемия);
- Нехватка питания для клеток мозга по причине гипоксии;
- Причины, которые вызваны целым рядом заболеваний.
Этиология патологии Бинсвангера — лейкоэнцефалопатия
Этиология заболевания лейкоэнцефалопатия делится на:
- Этиологию врождённого характера;
- Приобретённый тип этиологии заболевания.
Врождённая этиология лейкоэнцефалопатии — это аномалия в период внутриутробного формирования клеток головного мозга будущего малыша.
Причинами внутриутробного не правильного формирования плода могут быть:
- Недостаток кислорода, который спровоцировал гипоксию клеток головного мозга;
- Инфекционные заболевания у беременной женщины;
- Вирусы, что посредством плацентарной связи попали от матери к развивающемуся ребёнку;
- Если у матери имеется патология иммунодефицита.
Приобретенная этиология лейкоэнцефалопатии может быть при таких болезнях-провокаторах:
- Последствия травмирования клеток мозга;
- Влияние на мозг токсинов;
- После патологии — лучевая болезнь;
- При заболеваниях клеток печени, которые не выводят из системы кровотока все необходимые токсические вещества, что максимально загрязняют биологическую жидкость несущую данные элементы по системе кровоснабжения в головной мозг;
- При злокачественных новообразованиях в органах;
- При болезни лёгких, когда организм не дополучает необходимую дозу кислорода;
- При высоком индексе артериального давления — гипертоническая болезнь;
- При низком индексе артериального давления — гипотония;
- СПИД;
- Лейкоз клеток крови;
- Раковые новообразования в составе крови;
- Патология лимфогранулематоз;
- Туберкулез лёгкого;
- Заболевания онкологического характера — саркоидоз;
- Метастазирования раковых клеток в печеночный орган и в головной мозг.
Поражение белого вещества мозга при лейкоэнцефалопатии
Виды патологии
К данной классификации относятся группы патологии лейкоэнцефалопатии. Так как причин данного заболевания множество, поэтому и разновидности данной патологии, тоже имеют свои характерные отличия по этиологии, по своему проявлению и течению.
Можно условно разделить на 3 типа лейкоэнцефалопатии:
- Лейкоэнцефалопатия сосудистого характера;
- Патология гипоксического — ишемического типа;
- Лейкоэнцефалопатия геморрагического типа.
Но часто встречается диффузная многоочаговая форма заболевания.
Лейкоэнцефалопатия сосудистого характера
Причиной сосудистой лейкоэнцефалопатии является гипоксия мозговых сосудов, а также их ишемия. Данная этиология подразумевает неполноценное выполнение своих функций сосудами мозга. Нарушения функциональности мозговых сосудов чаще всего провоцируют нарушения, или же патологии в системе кровотока организма.
В связи с данной этиологией, существует несколько подвидов лейкоэнцефалопатии сосудистого характера:
Лейкоэнцефалопатия венозного типа.
К этому типу патологии приводит плохая циркуляция венозной крови ( что это за вид крови). Данный тип заболевания относится к лёгкому и длительному периоду развития. От момента первой симптоматики может пройти несколько календарных лет до очередного этапа развития болезни.
При начальной стадии в легкой степени лейкоэнцефалопатии проводится медикаментозный лечебный курс терапии, который может навсегда избавить больного от патологии.
При запущенной стадии, осложнённая форма заболевания развивается довольно быстро и приводит к необратимым и не излечимым последствиям.
Лейкоэнцефалопатия атеросклеротического характера.
Причиной данной разновидности патологии, является атеросклероз артерий. Холестерин образовывает атеросклеротические бляшки на стенках артерий, что приводит к плохому движению по сосудам крови, или же происходит закупорка артерий.
У пожилых пациентов атеросклероз может развиться вследствие не правильной работы органов пищеварительной системы, или от не соблюдения культуры питание — употребление большого количества холестерин содержащих продуктов питания.
При закупоривании мозговых сосудов начинается кислородное голодание клеток мозга. Излечить данный тип патологии можно только при диагностировании ее на ранней стадии возникновения.
Если атеросклеротическая лейкоэнцефалопатия не диагностирована своевременно, она может развиваться стремительно и очень быстро перейти в осложнённую форму, и привести к необратимым процессам в головном мозге и в организме. Это патология субкортикальная атеросклеротическая лейкоэнцефалопатия.
Лейкоэнцефалопатия гипертонического типа.
Провокаторами данного типа патологии могут быть: эклампсия сосудов, нефрит почечного типа в острой фазе развития болезни, скачки индекса артериального давления, а также самый опасный провокатор, это гипертонический криз.
Гипертонический криз вызывает острую форму энцефалопатии, что сразу же приводит к необратимым последствиям состояния головного мозга.
Предсказать данный вид течения патологии невозможно. Лейкопатии сосудистого генеза имеет схожую симптоматику с патологией дисциркуляторная энцефалопатия. Точный диагноз лейкоэнцефалопатии, которая выявлена мелкоочаговая вероятно сосудистого генеза, может поставить профильный доктор — невролог, после комплексного диагностического изучения этиологии.
Медикаментозная терапия будет проводиться исходя из диагноза и формы течения патологии.
Лейкоэнцефалопатия гипоксического-ишемического типа
Любую лейкоэнцефалопатию сосудистого характера можно отнести и к типу гипоксически-ишемическому, так как каждая из сосудистых типов патологии приводит к гипоксии головного мозга, что провоцирует лейкоэнцефалопатию.
Но данный тип патологии выделен в отдельную категорию при классификации, по причине того, что лейкоэнцефалопатия является осложнённой формой тяжёлых родов у новорождённых малышей.
Гипоксически-ишемический тип энцефалопатии возникает у ребенка в период внутриутробного его формирования, а также при осложнении в период родового процесса.
Развитие данной патологии протекает не предсказуемо, и последствия так же бывают разными. Минимальная потеря функциональности головного мозга у детей может привести к невнимательности малыша, с невозможностью сконцентрироваться и запоминать нужную информацию — это лёгкая степень последствий гипоксически-ишемического типа патологии.
Более тяжёлые осложнения приводят к полному параличу организма ребёнка.
К гипоксически-ишемическому типу очагов лейкопатии в головном мозге можно отнести и перинатальную форму лейкоэнцефалопатии.
Данная энцефалопатия развивается по принципу взрослого заболевания, только существует единственная разница — ее возникновение произошло в утробе матери, или же в первое время сразу после момента рождения.
Геморрагический тип лейкоэнцефалопатии
Данный тип патологии мозга возникает от авитаминоза клеток мозга. Недостаток витамина тиамин приводит к развитию мультифокальной лейкоэнцефалопатии геморрагического характера.
Данный тип патологии протекает так же, как происходит развитие других типов энцефалопатии, но этиологией данного типа, являются:
- Патология в пищеварительной системе, которая спровоцировала анорексию;
- Длительный рвотный рефлекс и большое количество рвотных отделений из организма;
- Гемодиализ;
- Синдром приобретённого иммунодефицита (СПИД).
Прогрессирующая мультифокальная лейкоэнцефалопатия
Данная патология относится к смертельно опасным видам болезни и вызвана папилломавирусом. Довольно часто приводит к смертельному исходу. Это патология, которая развивается более чем у 50,0% больных СПИДом.
Прогрессирующая многоочаговая форма лейкоэнцефалопатии проявляется:
- Паралич тела;
- Гемианопсия одностороннего типа;
- Парез периферического отдела;
- Дефект сознания личности;
- Синдромы экспирамидных видов.
Инвалидизация при данном типе патологии приходит довольно быстро, так как ее развитие происходит стремительно на фоне сниженного иммунитета. Происходит снижение функциональности двигательного аппарата, речевого и слухового аппарата.
В период прогрессирования болезни происходит паралич частей тела и частичный паралич мозга.
Поражение мозга при прогрессирующей мультифокальной лейкоэнцефалопатии
Перивентрикулярная форма
Данный тип патологии происходит от гипоксии мозга при хронической недостаточности крови в мозговых сосудах. Участки ишемического поражения находятся не только в белом мозговом веществе, но и в клетках серого вещества.
Локализация данного разрушения происходит в:
- Мозжечке;
- Двухсторонняя патология в лобных отделах коры головного мозга;
- В стволе мозгового органа.
Все отделы мозга, которые подвержены поражению, влияют на развитие двигательных функций. Расстройство данных участков приводит к парализации некоторых частей тела.
У новорождённых детей данный тип лейкоэнцефалопатии развивает патологию — детский церебральный паралич. Это происходит через несколько часов после рождения ребенка.
Лейкоэнцефалопатия, при которой исчезает белое мозговое вещество
Данный тип диагностируется в детском возрасте от 2 календарных лет до 6-летия. Происходит такое исчезновение в коре головного мозга по причине мутации генов. Данная патология имеет единичный неспецифический очаг, или же мелкофокусные очаги, которые поражают все отделы мозга.
Симптоматика данного вида:
- Нет координации в движении;
- Парез конечностей;
- Снижение памяти, или же ее утрата;
- Нарушение зрения — атрофируется нерв зрительного органа;
- Приступы эпилепсии.
У таких детей происходит проблема с потреблением пищи, они сильно возбудимы, а также имеют повышенный мышечный тонус.
Проявляется патология в апноэ, мышечных судорогах и в коматозном состоянии, которое часто заканчивается летальным исходом.
Сколько живут при лейкоэнцефалопатии?
Данная патология является самой опасной болезнью клеток головного мозга. При стабильном течении патологии время жизни отмеряно по медицинским прогнозам чуть больше, двух календарных лет.
При остром течении заболевания, которое сразу перешло в осложнённую форму — не более 30 календарных дней.
Средний показатель жизни при поставленном диагнозе лейкоэнцефалопатия — не более 6 календарных месяцев, с момента установления точного типа диагноза патологии. В данной болезни время может решить исход жизни — в положительную сторону, или же привести к смерти.
Чем быстрее проведена диагностика и найдена причина заболевания, тем быстрее можно начать терапию и спасти человеку жизнь.
Прогноз
Для мультифокальной прогрессирующей лейкоэнцефалопатии характерно неуклонное усугубление клинической картины – неврологическая симптоматика утяжеляется, вплоть до появления комы.
В настоящее время заболевание признается специалистами неизлечимым. Продолжительность жизни составляет при острой форме не более 10-12 месяцев от момента постановки диагноза.
Прогноз может считаться относительно благоприятным при своевременном распознавании патологии, принятии адекватных лечебных мер – подъем иммунитета, мощная противовирусная терапия.
На прогноз оказывают влияние факторы:
- возраст,
- исходное состояние его здоровья,
- сопутствующие заболевания,
- доступность специализированной медицинской помощи,
- квалификация врача, занимающегося лечением,
- эффективность проводимой терапии и реакция на нее иммунной системы человека.
В ряде случаев врачам удавалось продлить человеку жизнь до 2.5-3 лет, но отмечалось и молниеносное течение болезни – летальный исход к концу месяца от начала лейкоэнцефалопатии.
Особенности заболевания
Лейкоэнцефалопатия — это неизлечимое заболевание головного мозга, которое поражает его белое вещество. Данная патология — это очаговое поражение, а также многоочаговое поражение белого вещества в составе мозга.
Этиология заболевания — это вирусы, которые несут разрушительный характер для организма и в первую очередь поражают клетки головного мозга.
Возникновение патологии происходит от сниженной функциональности иммунной системы, преимущественно у людей глубоко преклонного возраста, а также при поражении организмом патологией иммунодефицита. При СПИДе лейкоэнцефалопатия развивается в любой возрастной категории.
Существует проблема в медикаментозной лечебной терапии данного типа болезни мозга.
Все дело в том, что в головном мозге существует барьер, через который могут попасть в клетки мозга, только препараты, содержащие в основе жиры.
Данные жирорастворимые лекарственные средства способны повлиять на клетки головного мозга, но препараты, которые способны эффективно, и в довольно быстрые сроки излечить лейкоэнцефалопатию, находятся на основе воды. Водорастворимые медикаменты, не способны преодолеть мозговой барьер.
Поэтому на сегодняшний день фармакологические компании не смогли разработать препараты для медицинской эффективной помощи патологии — лейкоэнцефалопатия.
Тактика лечения
В связи с трудностями своевременного распознавания мультифокальной прогрессирующей лейкоэнцефалопатии, особенностями механизма ее появления и течения, специфического лечения в настоящее время не разработано.
Специалистами предпринимались попытки подавления вирусной активности разными подгруппами медикаментов — интерферонами, иммуностимуляторами. В ряде случаев положительный результат достигался после приема Цитарабина. Однако, многочисленные попытки достичь стойкого продолжительного результата успеха не имели.
Тем не менее, врачи ищут новые методы борьбы с вирусной патологией — к примеру, с помощью антидепрессанта Миртазапина. Препарат блокирует распространение вирусных частиц в клетки нейроглии.
Предпринимались попытки применения:
- противовирусных препаратов,
- противоопухолевых медикаментов,
- антагонистов серотониновых рецепторов.
Значимых показателей улучшения состояния иммунной системы не наблюдалось. Попытки трансплантации стволовых клеток костного мозга не дали желаемых результатов.
Отдельной группой специалистов признается действенным метод восстановления клеточного иммунитета у людей с аутоиммунным вариантом появления болезни за счет снижения доз иммунодепрессантов. Иногда удается полностью отменить терапию подобными лекарствами.
Исключением является состояние после трансплантации органов. В подтверждение врачи приводят случаи выраженного регресса негативной симптоматики, и даже выздоровление пациентов после отмены средств из подгруппы цитостатиков.
Признаки развития лейкоэнцефалопатии
Признаки многих типов лейкоэнцефалопатии проявляются постепенно. В начале развития появляются приступы забывчивости, рассеянности. Человек испытывает трудности в запоминании информации, в произношении длинных и сложных слов.
Появляется постоянное чувство жалости к себе, и больной много плачет. Интеллектуальная работоспособность мозга значительно снижается.
В дальнейшем развитии патологии появляется бессонница, которая может чередоваться с бесконечным желанием спать. Повышается тонус мышц, что в совокупности приводит к беспочвенной раздражительности больного.
На данном этапе развития болезни появляется сильный шум в ушах, а также непроизвольное подёргивание зрительного нерва, что приводит к необоснованному движению зрачков.
Если не начать комплексную терапию хоты бы на этом этапе, тогда болезнь приведёт до:
- Патологии психоневроза;
- К судорогам мышечных волокон;
- К слабоумию;
- К частичной потере памяти;
- К патологии деменция.
Симптомы лейкоэнцефалопатии
Симптомы данной патологии развиваются внезапно и прогрессируют в быстром темпе, что может привести больного к таким признакам заболевания:
- Паралич бульбарного типа;
- Синдром Паркинсона;
- Нарушена походка;
- Происходит тремор рук;
- Проявляются признаки дрожания тела.
Пациенты с такой симптоматикой не осознают о своей патологии и о поражении мозга, поэтому своевременно необходимо родственникам заставить таких людей пройти диагностирование, чтобы знать, как лечить заболевание.
Диагностика
Чтоб установить диагноз лейкоэнцефалопатия клеток тканей головного мозга, необходимо пройти ряд диагностических исследований:
- Визуальный осмотр доктора невролога и сбор анамнеза;
- Лабораторный клинический анализ крови (общий);
- Анализ состава крови на присутствие в ней психотропных элементов, алкоголя, и наркотиков содержащих веществ;
- МРТ и КТ (томографии – компьютерная, или магнитно-резонансная) для выявления очага в отделах головного мозга;
- Инструментальная диагностика методом электроэнцефалографии, позволит выявить снижение мозговой активности клеток органа;
- Допплерография — это методика, при которой выявляется патология, и нарушения в системе кровотока, а также мозговых сосудах;
- ПЦР анализ на выявление вируса в составе организма. По данному анализу определяется ДНК вируса-провокатора;
- Биопсия клеток головного мозга;
- Пункция цереброспинальной жидкости.
Если выявляется, что провокатором лейкоэнцефалопатии есть вирусы, тогда проводится еще диагностика методом электронной микроскопии клеток головного мозга.
Допплерография сосудов головы
Дифференциальное диагностическое исследование проводят при следующих патологиях:
- Заболевание токсоплазмоз;
- Патология криптококкоз;
- Деменция при ВИЧ;
- Заболевание лейкодистрофия;
- Болезнь лимфома ЦНС;
- Патология панэнцефалит склерозирующий подострого типа;
- Рассеянный вид склероза.